蹲到腿麻、胀到心烦、使劲到出汗......结果还是“一无所获”?
如果你也经历过这些,别怀疑,你不是一个人。便秘,这个让人羞于启齿的尴尬困扰,正在困扰全球近15%的人。
近日,华大营养钟一祎博士研发团队联合华大研究院邹远强博士团队,有关副干酪乳酪杆菌BGI-N2的最新研究成果正式发表于国际知名微生物学期刊BMC Microbiology。本研究首次从基因组到表型系统解析了BGI-N2缓解便秘的分子机制,为便秘的微生态干预提供了科学基础。

近年来研究发现,便秘的根源,通常藏在肠道里——有益菌在减少,捣乱的致病菌却越来越多。
这时,补充益生菌就像给肠道派去一支“维和部队”,它们能压制坏菌、调节肠道环境、唤醒肠道动力。但是,益生菌也是“一菌一世界”,不同菌株的效果天差地别。所以,找到一株真正能打、安全可靠的种子选手,就成了科研攻关的关键。
在此背景下,华大研发团队从健康人体肠道中筛选出副干酪乳酪杆菌BGI-N2,通过全基因组测序、体外功能验证、体内机制研究等多种策略,全面解锁了这株菌株缓解便秘的益生潜力和分子机制。
01
基因解码BGI-N2
藏在DNA里的⌈硬实力⌋
一株优秀益生菌的功能,早已刻在它的基因密码中。依托华大自主研发的CycloneSEQ 长读长测序平台,华大团队完成了BGI-N2的高精度完整基因组测序,为解析其益生功能提供了精准的基因基础。
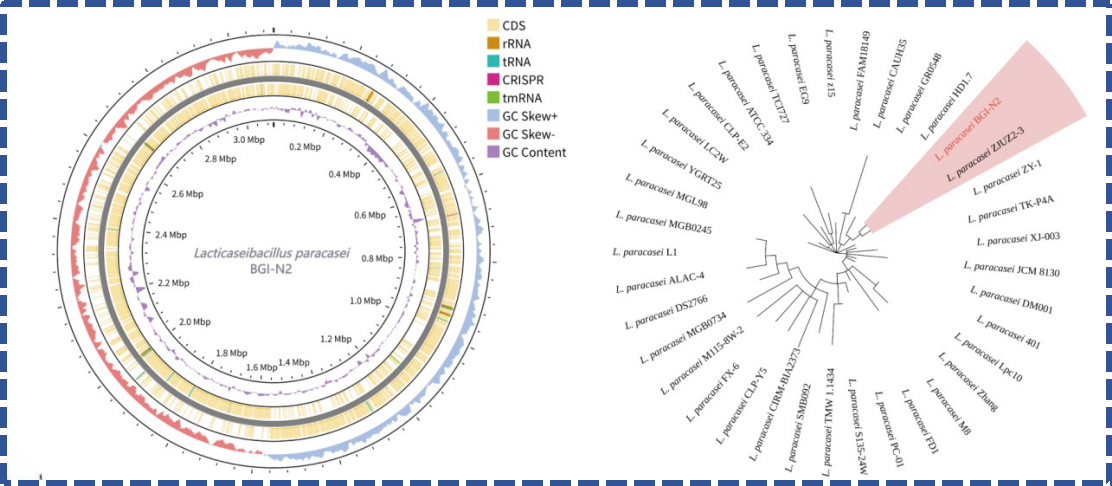
✅ 安全无虞,符合益生菌应用标准
基因组分析显示,BGI-N2无质粒存在,无致病性毒力基因,为后续应用筑牢安全防线。
✅ 超强消化耐受,顺利闯过人体“消化关卡”
BGI-N2基因组中富集了耐酸、耐胆盐、耐溶菌酶的相关功能基因,能通过维持质子稳态、调节膜稳定性、修饰细胞壁等方式适应胃肠道的极端环境。体外实验验证显示,其在人工胃液、肠液、0.3%胆盐溶液中的存活率均超90%,能顺利抵达肠道发挥作用
✅ 高效抑菌,重塑肠道健康微生态
BGI-N2基因组中含有乳酸、过氧化氢、双乙酰等抗菌物质的合成基因,还鉴定出萜类前体、RiPP样等次级代谢产物基因簇,此外还包含细菌素合成基因lcnD。体外抑菌实验中,BGI-N2对大肠杆菌、金黄色葡萄球菌、阴沟肠杆菌、铜绿假单胞菌等常见肠道致病菌均有显著抑制效果,最高抑制率达99%,能有效抑制致病菌增殖,优化肠道菌群结构。
✅ 优异肠道定植,长效发挥益生作用
BGI-N2携带mapA、lspA等多个黏附相关基因,还拥有应激响应等肠道适应相关基因,能通过结合肠道粘蛋白、适应肠道环境实现稳定定植。在斑马鱼模型中,BGI-N2的24小时肠道滞留率高达83.37%,为其长效缓解便秘提供了重要保障。
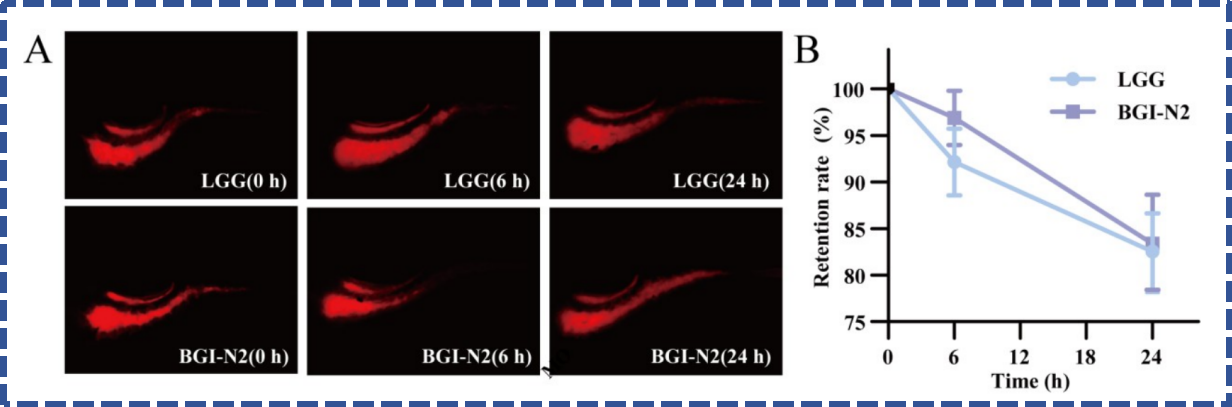
02
体内研究实证
BGI-N2显著改善便秘症状
为验证BGI-N2的体内便秘缓解效果,华大团队选用斑马鱼作为实验模型,通过构建斑马鱼便秘模型,设置低、中、高三个剂量的BGI-N2干预组,同时设置正常对照、模型对照和阳性药对照,通过尼罗红荧光标记法检测肠道内容物滞留情况,评估肠道动力。
实验结果十分亮眼,模型组斑马鱼肠道内容物显著堆积,而经BGI-N2干预后,中、高剂量组斑马鱼肠道内容物量显著降低,肠道动力和排空能力得到明显提升,便秘症状得到有效改善,且在实验浓度范围内,BGI-N2对斑马鱼无急性毒性,进一步印证了其安全性。
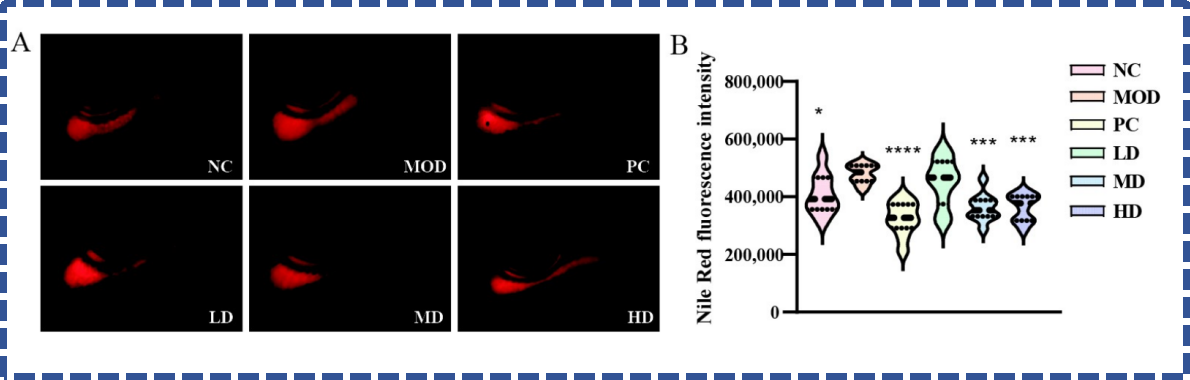
03
深挖机制
BGI-N2 缓解便秘的三重⌈杀手锏⌋
华大团队进一步从分子层面解析了BGI-N2 缓解便秘的核心机制,发现其通过多靶点、多通路调控肠道动力,实现便秘缓解,这也是本研究的核心创新点。
杀手锏1:下调肠道NO水平
解除肠道动力抑制
一氧化氮(NO)是肠道内的抑制性神经递质,过量合成会直接导致肠道蠕动迟缓,是便秘发生的重要诱因。BGI-N2能剂量依赖性降低便秘斑马鱼肠道的NO浓度,解除NO对肠道平滑肌的抑制作用,让肠道动力恢复正常。
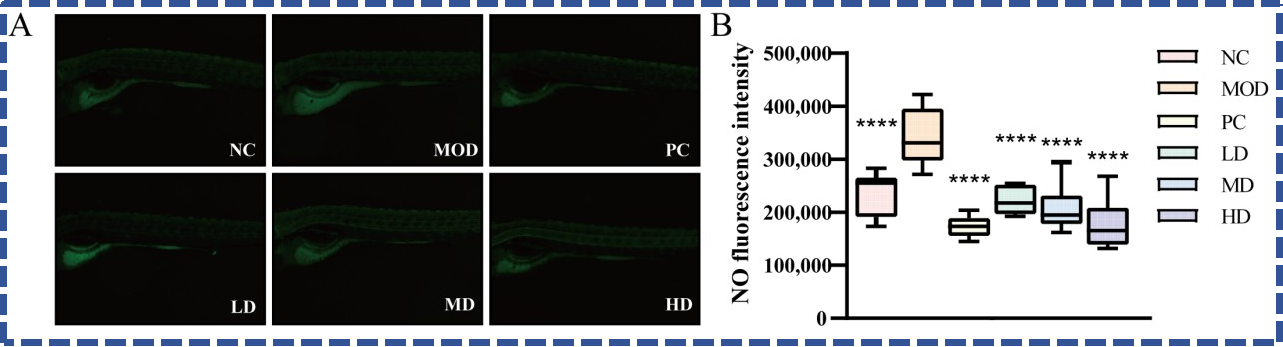
杀手锏2:激活Kit通路
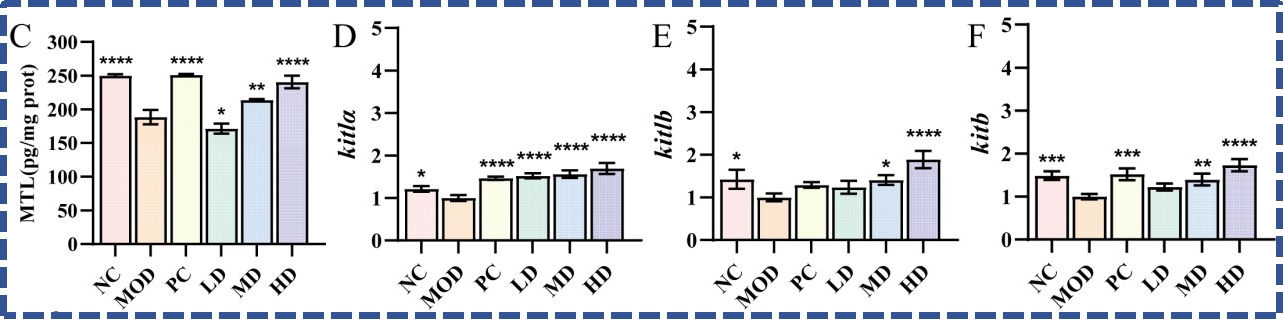
提升MTL水平,筑牢肠道“起搏系统”
肠道的正常蠕动离不开“起搏细胞”(卡哈尔间质细胞),它能调控肠平滑肌的节律性收缩,而Kit信号通路(kitla/kitlb/kitb)是其发育、维持功能的核心。
BGI-N2能显著上调kitla、kitlb、kitb基因的表达,促进“起搏细胞”的发育和功能维持。同时还能提升斑马鱼体内胃动素水平,胃动素作为经典的促动力激素,能直接刺激肠平滑肌收缩,双重作用下筑牢肠道的动力起搏系统。
杀手锏3:多维度调控5-HT
放大肠道蠕动信号
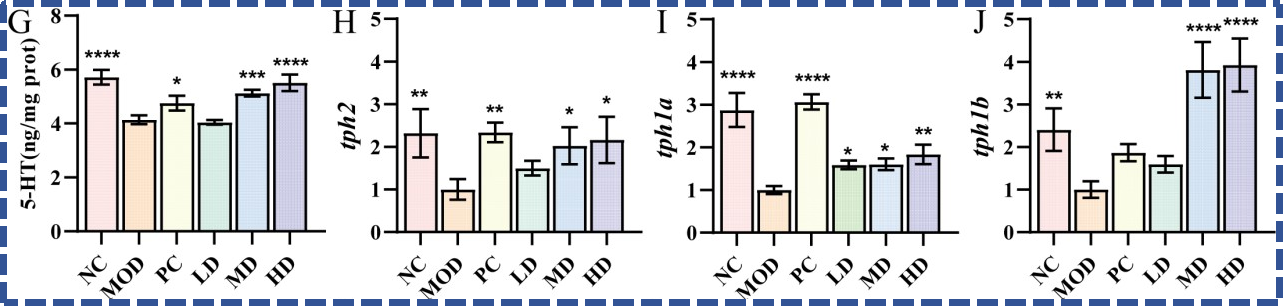
5-羟色胺(5-HT)是调节肠道蠕动和分泌的核心神经递质,其含量不足会直接导致肠道蠕动信号传导受阻。BGI-N2通过三重调控实现肠道5-HT的有效蓄积:
促进合成:上调5-HT合成限速酶相关基因tph1a、tph1b、tph2的表达,加速5-HT生成;
减少转运:下调5-HT转运基因sert的表达,降低5-HT的重吸收,让更多5-HT发挥作用;
增强感知:上调5-HT受体基因htr1aa的表达,提升肠道细胞对5-HT的敏感性。
三者协同,让肠道 5-HT 水平显著提升,有效促进肠道蠕动反射,改善便秘。
本研究首次对副干酪乳酪杆菌 BGI-N2进行的全基因组解析+功能验证+机制挖掘,从基因到表型,系统阐明了BGI-N2缓解便秘的益生潜力和分子机制。
未来,华大将继续深耕肠道微生态与人体健康领域,开展更多益生菌的功能挖掘和机制研究,开发更多贴合大众健康需求的益生菌产品,用微生态科技守护大众健康!