近日,华大旗下益生菌植物乳植杆菌BGI-N6在微生物领域国际期刊Microbiological Research(IF=6.9)发表最新研究成果,首次系统揭示了其通过调节肠道菌群及其代谢物,多维度缓解高脂饮食诱导的肥胖、炎症与氧化应激的作用机制。

《2025世界肥胖地图》显示,中国成年人中超重比例已达41%,肥胖率为9%。[1]若采用我国本土标准(BMI≥24为超重),这一数字更为严峻。
2026年世界肥胖日主题提出“80亿个理由行动起来应对肥胖”,向全球80亿人发出行动呼吁,同心协力,共同面对肥胖带来的疾病负担与健康挑战。
面对这一挑战,我们更需追问,是哪些因素导致全球肥胖危机,是饮食习惯、食品环境,还是生活方式出了问题?我们又该如何从根源入手,扭转困局?
答案之一,就藏在我们的肠道里。
01
肥胖不仅是体重问题
更是“炎症”问题
科学研究早已揭示,肥胖本质上是一种慢性低度炎症状态。这种全身性的炎症和伴随的氧化应激,是连接肥胖与多种并发症的核心病理机制。
而点燃这把“火”的,往往是失衡的肠道菌群。
高脂饮食、作息紊乱、环境压力,都会导致肠道内有害菌增多、有益菌减少,内毒素(LPS)进入血液,激活全身免疫系统,形成“炎症-肥胖-更严重的炎症”的恶性循环。
02
BGI-N6:多管齐下,精准灭火
破解肥胖代谢难题
那么,有没有可能通过调节肠道菌群,从源头“灭火”,打破肥胖的恶性循环?
华大自主研发的植物乳植杆菌BGI-N6,正是为此而生。
本次研究的植物乳植杆菌BGI-N6为华大自主筛选的人源菌株,研究团队以高脂饮食诱导的SD大鼠为模型,设置低、高剂量BGI-N6 干预组,系统探究其对肥胖及代谢紊乱的改善效果。实验结果显示,BGI-N6展现出显著的抗肥胖及代谢调节能力:
有效抑制体重增长与脂肪沉积
BGI-N6干预后大鼠体重、体重增幅显著降低,附睾脂肪、肾周脂肪及总脂肪指数下降,脂肪细胞体积明显减小,且未改变大鼠食物摄入量,说明其并非通过减少进食发挥作用,而是调节了机体的能量利用效率。
改善肝脏脂代谢紊乱
BGI-N6显著逆转了高脂饮食引发的肝脏脂肪变性,降低肝脏重量指数与肝内脂质积累,缓解非酒精性脂肪肝样病变。
纠正糖脂代谢异常
BGI-N6降低了大鼠空腹血糖、胰岛素水平,改善胰岛素抵抗(HOMA-IR),同时下调了血清甘油三酯、总胆固醇、低密度脂蛋白胆固醇,让紊乱的糖脂代谢重回正轨。
缓解炎症与氧化应激
BGI-N6显著降低了血清促炎标志物C反应蛋白(CRP)、肿瘤坏死因子α(TNF-α)水平,上调了抗炎细胞因子IL-10,同时恢复了血清及肝脏中超氧化物歧化酶(SOD)、谷胱甘肽过氧化物酶(GSH-Px)的抗氧化活性,打破肥胖引发的“炎症-氧化应激”恶性循环。
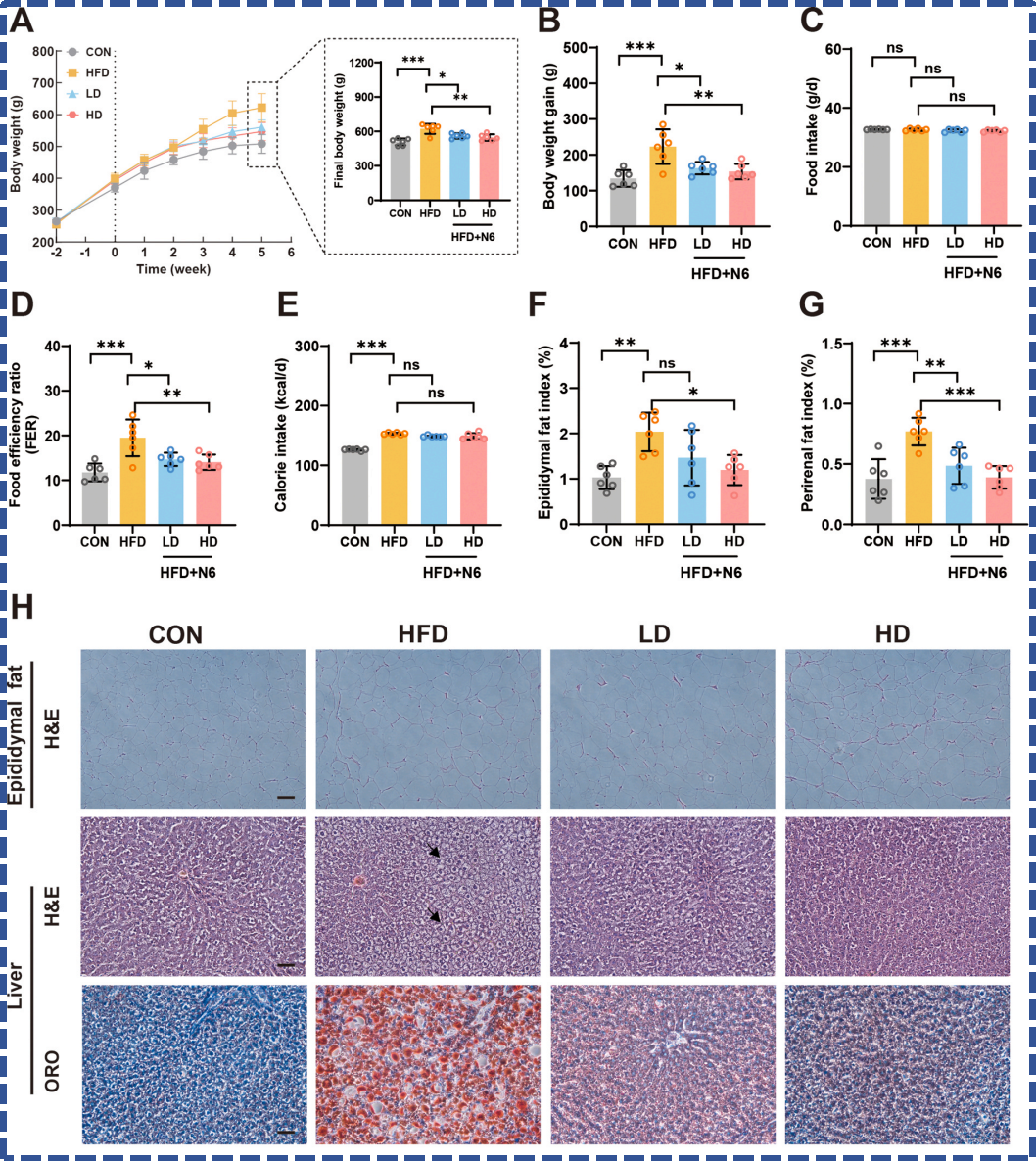
🔼 BGI-N6通过减少大鼠能量摄入和脂质积累来缓解高脂饮食引起的肥胖
03
深入机理:多机制协同
解锁BGI-N6的抗肥胖密码
研究团队进一步通过宏基因组测序、靶向代谢组检测等多组学技术,深入解析了BGI-N6发挥益生作用的分子机制,发现其并非单一靶点调节,而是通过重塑肠道菌群、调节代谢物平衡、抑制LPS介导的炎症通路等多途径协同作用,实现对肥胖相关代谢紊乱的改善。
机制1:重塑肠道菌群结构
逆转高脂饮食诱导的菌群失调
肠道菌群失调是肥胖发生发展的重要诱因,高脂饮食会导致肠道菌群组成失衡,促炎菌丰度升高。BGI-N6的干预显著提升了菌群β多样性,让紊乱的肠道菌群结构向正常状态恢复;同时特异性降低了促炎菌的丰度(如Sutterella wadsworthensis、Bilophila wadsworthia、Holdemania filiformis等),这些菌株是引发肠道炎症、破坏肠道屏障的关键菌,其丰度降低为宿主代谢健康奠定了基础。
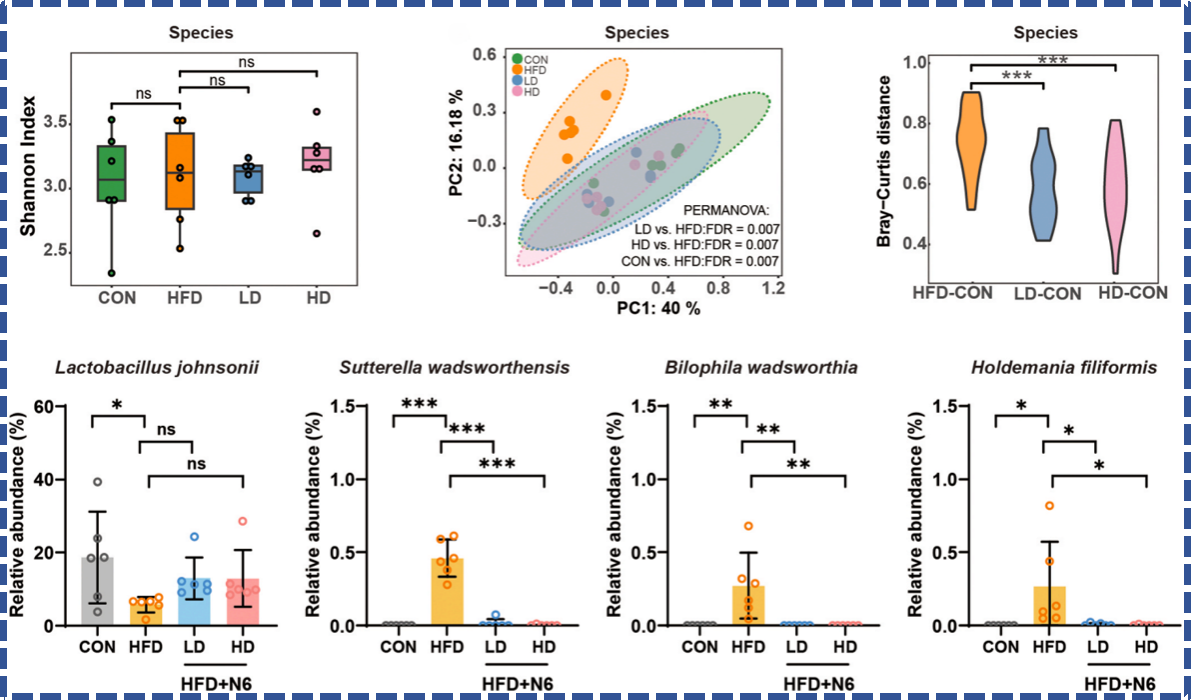
🔼 BGI-N6补充重塑了高脂饮食大鼠的肠道微生物群组成和多样性
机制2:调节短链脂肪酸代谢
恢复肠道代谢物平衡
短链脂肪酸(SCFAs)作为肠道菌群的核心代谢物,直接参与宿主能量代谢、炎症调节与肠道屏障维护。高脂饮食会导致大鼠粪便中总SCFA水平下降,丙酸升高、丁酸和戊酸降低,而BGI-N6干预精准纠正了这一失衡,显著提升了丁酸、戊酸水平,降低了丙酸水平。
相关性分析证实,丁酸、戊酸与体重增长、脂肪沉积、炎症指标呈负相关,而丙酸与上述指标呈正相关,说明BGI-N6能够通过调节SCFAs谱,从代谢物层面直接调控宿主的肥胖与炎症状态。
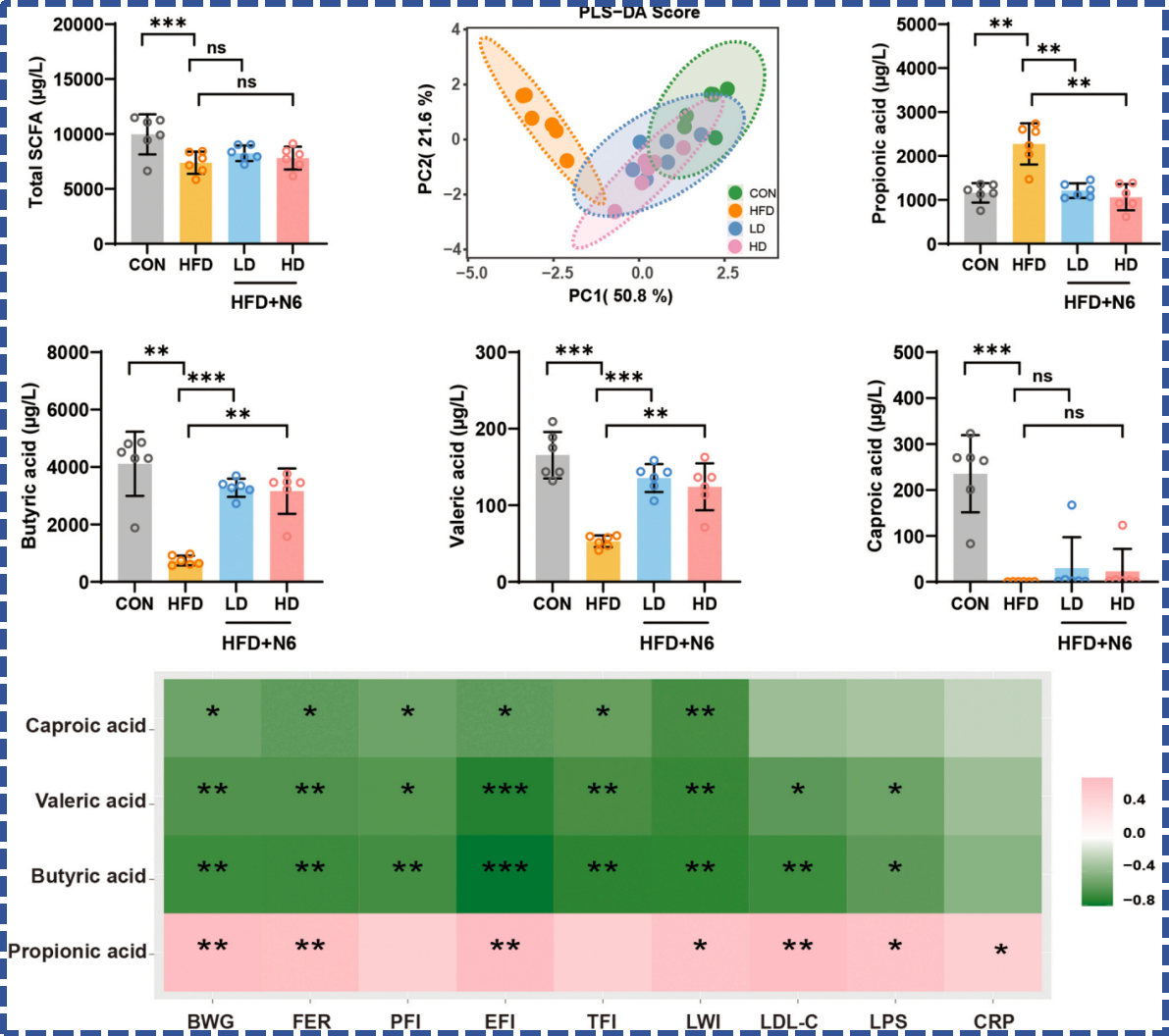
🔼 BGI-N6调节高脂饮食喂养大鼠的粪便短链脂肪酸谱
机制3:抑制LPS生物合成与全身转运
阻断炎症信号通路
脂多糖(LPS)是革兰氏阴性菌的细胞壁成分,被称为“内毒素”,高脂饮食会促进肠道菌群合成LPS并通过受损的肠道屏障进入血液,引发全身慢性炎症。BGI-N6通过降低促炎革兰氏阴性菌丰度,显著下调LPS生物合成相关通路,使大鼠血清LPS水平大幅降低;而血清LPS的降低直接减少了促炎细胞因子的释放,同时改善了胰岛素抵抗。
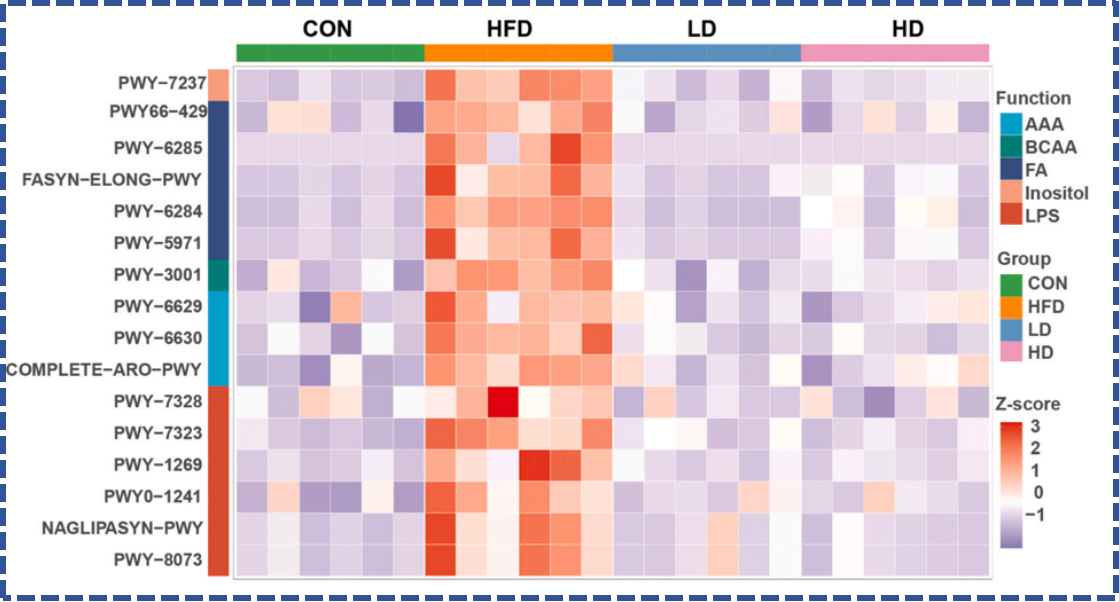
🔼 BGI-N6改善与肠道微生物群和脂多糖相关的高脂饮食引起的代谢失衡
本研究成果系统阐明了植物乳植杆菌BGI-N6的抗肥胖及代谢调节作用与机制,证实其通过肠道菌群-代谢物-宿主免疫的互作网络,多维度缓解肥胖相关的炎症、氧化应激与代谢紊乱,是一株极具开发潜力的功能性益生菌。(口服益生菌也能护肤?最新研究揭秘华大BGI-N6的美颜基因)
而华大营养凭借成熟的益生菌产业化研发体系,已将BGI-N6这一核心菌株成果,成功应用于【镜脂】系列益生菌产品中,实现了科研成果的快速落地。
未来,华大营养将继续深耕肠道微生态领域,结合多组学技术与临床研究,开发更多贴合国人肠道特征的益生菌产品,以科技赋能大众健康,为代谢性疾病的防控提供更多安全、有效的干预方案。